物创实验室科研团队JACS:揭示了唾液酸化修饰在保护蛋白质结构和功能免受氧化应激损伤中的分子机制
2025-02-14

物质绿色创造与制造海河实验室、南开大学李功玉课题组(研究方向:D蛋白质谱分析)与蔡文生/付浩浩课题组(研究方向:分子模拟与计算化学)合作,在美国化学会志JACS在线发表了题为“Sialylation Shields Glycoproteins from Oxidative Stress: Mechanistic Insights into Sialic Acid Oxidation and Structural Stability”的研究论文。本研究通过自主搭建的非变性绿色氧化装置、非变性离子淌度质谱设备和结构质谱指引的分子建模平台,发展了《高性能构象分辨质谱》新方法。该方法首次揭示了唾液酸化修饰在保护蛋白质结构和功能免受氧化应激损伤中的分子机制,为理解糖基化在细胞应激中的作用提供了新视角,并为开发更稳定的蛋白质药物开辟了创新方向。
以下为转载南开化学公众号内容研究背景
唾液酸化是一种常见的蛋白质翻译后修饰,广泛存在于糖蛋白的末端。它在细胞间通信、细胞分化、免疫反应等多种生命活动中发挥重要作用。然而,氧化应激会导致蛋白质的结构破坏和功能失调,从而引发包括癌症、神经退行性疾病(如帕金森病和阿尔茨海默病)以及代谢紊乱在内的多种疾病。尽管唾液酸化被认为可以在一定程度上缓解这种损伤,其具体机制却一直未被完全阐明。
论文简介
近日,南开大学李功玉课题组(研究方向:D蛋白质谱分析)与蔡文生/付浩浩课题组(研究方向:分子模拟与计算化学)合作,通过自主搭建非变性绿色氧化装置、非变性离子淌度质谱设备和结构质谱指引的分子建模平台,发展《高性能构象分辨质谱》从小分子到完整蛋白大分子的跨尺度质谱分析新方法,首次揭示了唾液酸化修饰在保护蛋白质结构和功能免受氧化应激损伤中的分子机制,为理解糖基化在细胞应激中的作用提供了新视角,并为开发更稳定的蛋白质药物开辟了潜在的创新方向(J. Am. Chem. Soc. 2025, doi: 10.1021/jacs.4c14454)。
研究亮点
该工作是李功玉课题组在《构象分辨质谱分析》应用方法学创新开发的代表性成果,使构象分辨质谱技术从小肽的显著结构差异分析(Angew. Chem. Int. Ed. 2023; Chem. Sci. 2023; Anal. Chem. 2023)跨越至大蛋白的微小结构扰动分析(J. Am. Chem. Soc. 2025; Chem. Sci. 2024; Anal. Chem. 2023; Anal. Chem. 2022; Chin. Chem. Lett. 2024),有效提高了结构质谱解析气相蛋白动态构象的结构分辨率(Nat. Commun. 2019),成功破译翻译后修饰对完整糖蛋白的抗氧化密码,属于化学测量学领域质谱分析方向的前沿研究课题。
研究内容
本研究团队设计了一种微尺度低温等离子体(microLTP)装置,模拟了细胞中复杂的氧化应激环境,并结合高分辨率质谱分析和密度泛函理论(DFT)计算,首次完整绘制了两种常见唾液酸(Neu5Ac 和 Neu5Gc)在自由基氧化条件下的氧化路径图。研究发现,唾液酸的氧化过程呈现出独特的“逐步侧链氧化“模式,而非传统化学反应中常见的糖环断裂。这一新发现为唾液酸在保护蛋白质结构稳定性方面的作用提供了分子水平的解释。
进一步的研究以人转铁蛋白(hTF)为模型,结合酶学处理、离子淌度质谱(IM-MS)和液相色谱-串联质谱(LC-MS/MS),揭示了唾液酸化修饰如何通过特定的糖基化模式显著增强蛋白质在氧化应激下的结构稳定性。研究表明,唾液酸化修饰不仅能通过直接与活性氧(ROS)反应减少自由基对蛋白质主链的攻击,还能通过糖基屏蔽效应保护特定的蛋白质区域免受氧化损伤。
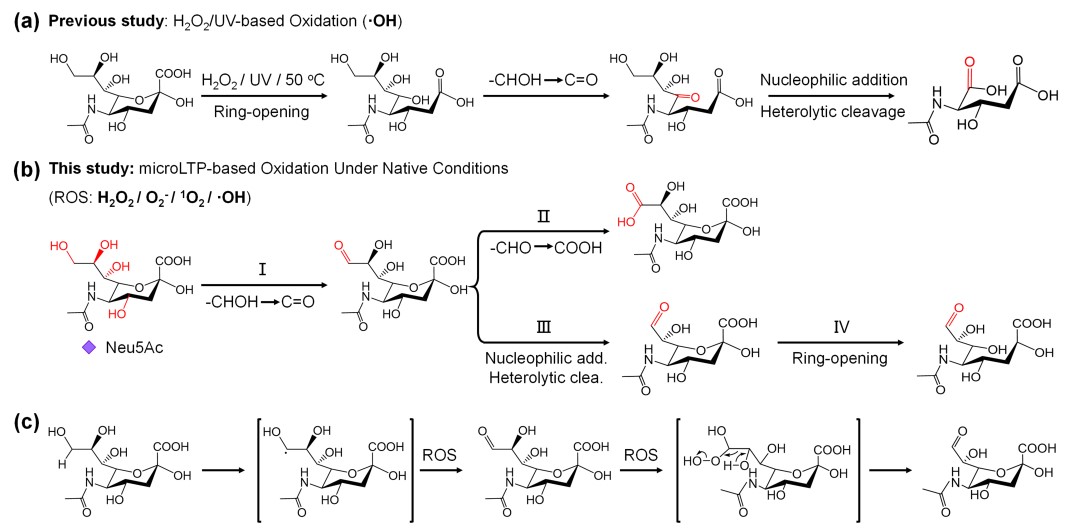
图1 唾液酸小分子的全新自由基氧化路径解析
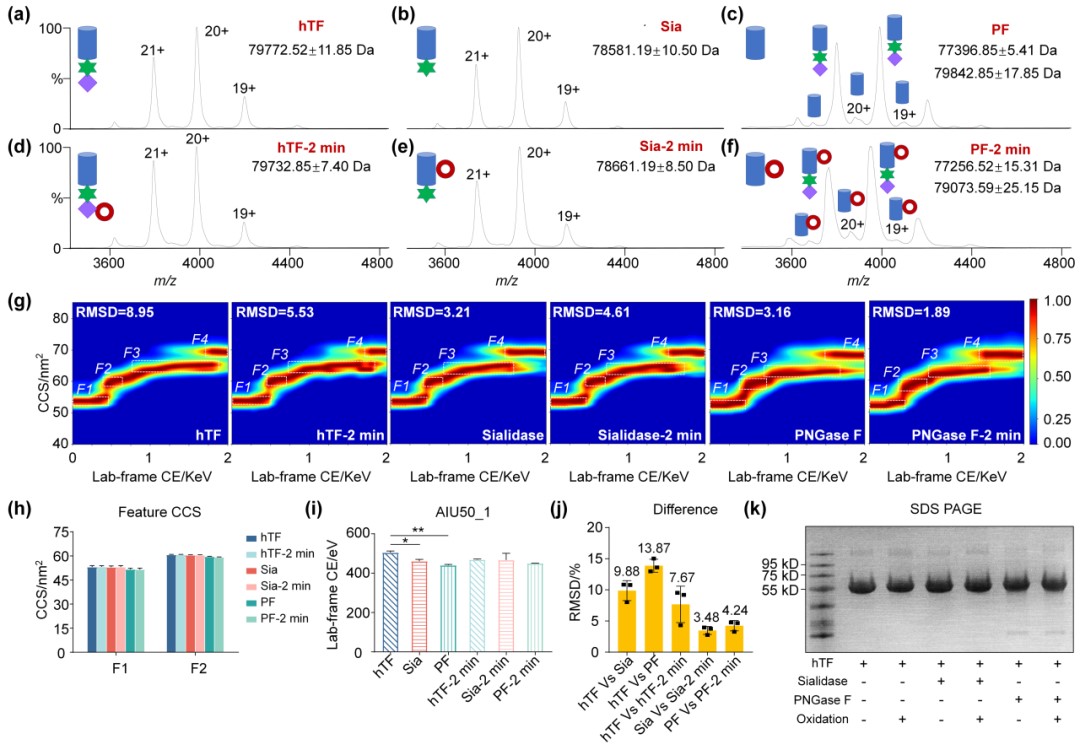
图2 完整糖蛋白大分子的结构质谱构象稳定性分析
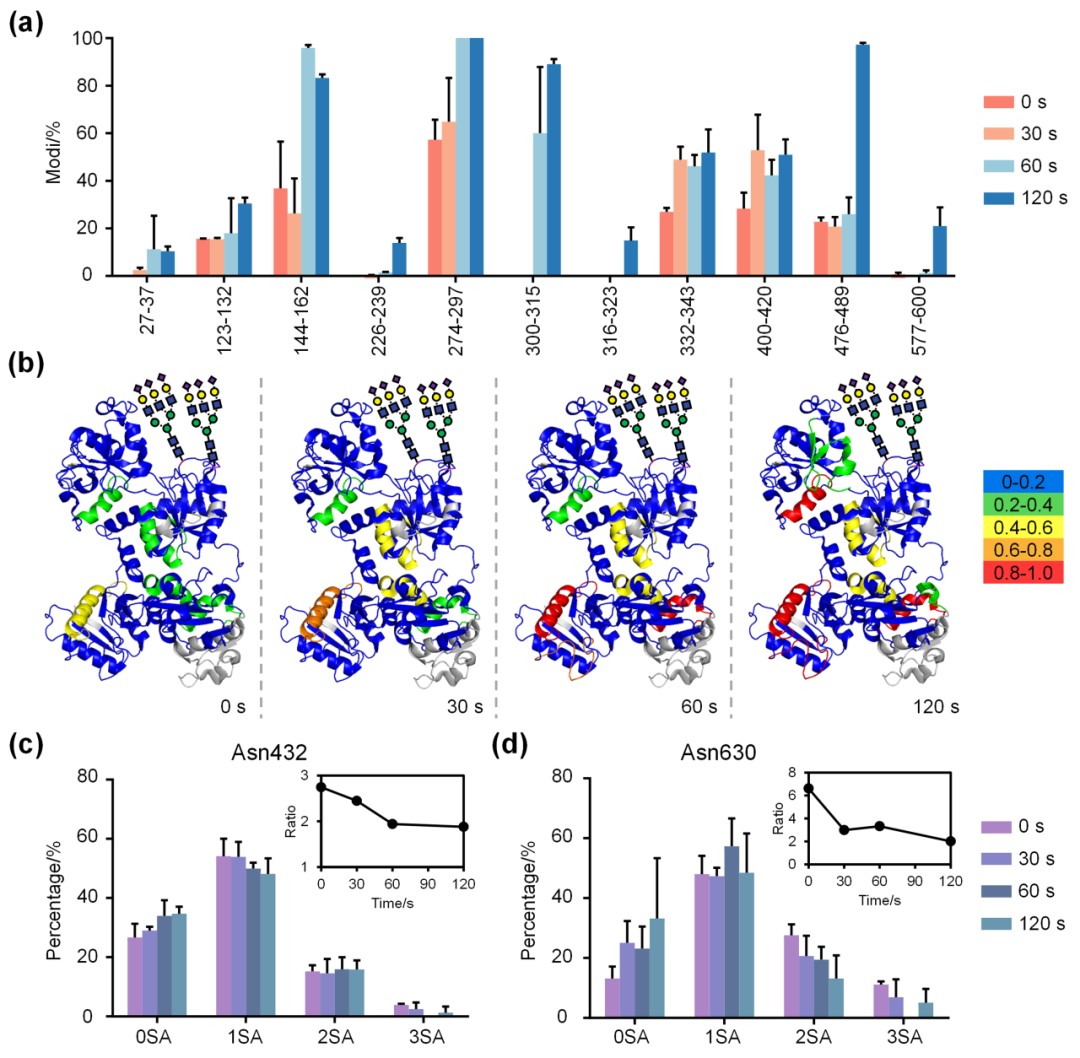
图3 完整糖蛋白大分子的抗氧化分子机制
这项研究具有重要的科学价值,不仅揭示了唾液酸化修饰在抗氧化应激中的独特作用,还为未来探索糖基化相关疾病(如癌症、神经退行性疾病和自身免疫病)的机制提供了新启示。以下是本研究的潜在应用前景:1)蛋白药物的稳定性提升:通过调控蛋白质的唾液酸化修饰,可以增强蛋白质药物在复杂生理环境中的稳定性,从而提高药物疗效并延长其使用寿命;2)疾病治疗的新靶点:深入研究唾液酸在糖基化相关疾病中的作用机制,有望开发出针对性更强的治疗策略,尤其是在缓解氧化应激相关疾病方面;3)新型抗氧化剂的开发:结合本研究揭示的唾液酸氧化路径,设计出基于糖基化的仿生抗氧化剂,可能为抗衰老和疾病预防领域带来突破。相关研究成果以《Sialylation Shields Glycoproteins from Oxidative Stress: Mechanistic Insights into Sialic Acid Oxidation and Structural Stability》为题在线发表于化学领域旗舰期刊Journal of the American Chemical Society (J. Am. Chem. Soc. 2025, doi: 10.1021/jacs.4c14454)。
南开大学化学学院2022级硕士研究生王雅梅、金东蓓为该文共同一作,李功玉研究员和付浩浩副研究员为本文共同通讯作者。美国威斯康星大学麦迪逊分校李灵军教授课题组张敬伟、天津医科大学刘阳平教授和郑珍教授对本项目提供了重要的技术支持。本文主要质谱数据均采集于天津《物质绿色创造与制造海河实验室》结构质谱分析平台。本研究工作获国家重点研发计划、国家高层次人才计划、国家自然科学基金和中央高校基本科研业务费等项目资助。
另附:南开大学李功玉课题组(详细信息请参考课题组主页:www.x-mol.com/groups/gongyu_li)常年招聘科研助理和师资博士后,欢迎对大分子结构质谱感兴趣的同仁联系(ligongyu@nankai.edu.cn),重点引进具有有机合成化学、计算化学、细胞生物学和蛋白质组学等背景的相关研究方向人才。
【分析化学博士招生】:课题组尚有1名2025年9月入学、质谱分析化学方向的博士研究生招生指标,欢迎符合南开化学申请考核基本要求(chem.nankai.edu.cn/2024/1023/c24089a553675/page.htm)并具有上述相关科研背景的学生报考。网上报名时间:2025年3月20日-4月10日。
论文信息
Sialylation Shields Glycoproteins from Oxidative Stress: Mechanistic Insights into Sialic Acid Oxidation and Structural Stability.
Yamei Wang, Dongbei Jin, Lifang Ren, Ning Wang, Yifei Jia, Zhen Zheng, Wensheng Cai, Haohao Fu* and Gongyu Li*
J. Am. Chem. Soc. 2025, xxxx.
https://doi.org/10.1021/jacs.4c14454
作者简介









